A triagem genética tem se consolidado como um instrumento relevante na prática médica preventiva, especialmente diante da evolução das tecnologias de sequenciamento genômico. Com a popularização do Sequenciamento de Nova Geração (NGS), tornou-se viável a análise ampla de genes associados a condições hereditárias de manifestação silenciosa, possibilitando a identificação precoce de riscos clínicos antes mesmo do surgimento de sintomas.
Esse modelo de abordagem preditiva ganha espaço quando confrontado com dados da Organização Mundial da Saúde (OMS), que estimam que até 40% dos casos de câncer podem ser prevenidos mediante estratégias adequadas, e cerca de 30% são potencialmente curáveis quando diagnosticados precocemente. Ainda assim, muitos diagnósticos continuam sendo realizados tardiamente, sobretudo em indivíduos sem antecedentes familiares relevantes, o que compromete o sucesso terapêutico.
Nesse contexto, o GenomaCare — Triagem Genética do Adulto, desenvolvido pelo Sabin, desponta como ferramenta de apoio clínico capaz de identificar variantes genéticas associadas a cânceres hereditários, cardiopatias genéticas e outras condições monogênicas clinicamente acionáveis. Trata-se de um exame de triagem voltado à investigação de risco em indivíduos assintomáticos, com potencial para embasar decisões clínicas personalizadas.
Aprofunde-se neste conteúdo e entenda como incorporar o GenomaCare à prática assistencial, com foco em medicina personalizada e diagnóstico precoce.
A importância da triagem genética na prática clínica
Diferentemente dos testes diagnósticos, que buscam confirmar uma condição clínica já suspeita ou sintomática, a triagem genética é indicada para indivíduos assintomáticos que desejam conhecer seu risco genético para doenças de base hereditária, permitindo ao médico antecipar estratégias de cuidado.
Essa abordagem é particularmente útil na detecção de variantes patogênicas associadas a doenças hereditárias de início tardio e progressão silenciosa, como cânceres e cardiopatias. Com base na identificação dessas variantes, é possível implementar medidas de rastreamento mais rigorosas, mudanças no estilo de vida, exames complementares e até intervenções redutoras de risco, como cirurgias e uso de fármacos moduladores.
É importante ressaltar que a seleção dos genes analisados no GenomaCare segue diretrizes clínicas internacionais atualizadas, em especial aquelas publicadas pelo American College of Medical Genetics and Genomics (ACMG) e pela base ClinGen, assegurando a relevância clínica e a confiabilidade dos achados.
O que é o GenomaCare — Triagem Genética do Adulto?
O GenomaCare é um exame de triagem genômica ampla, desenvolvido para identificar variantes associadas a doenças hereditárias que possuem condutas médicas bem estabelecidas. Por esse motivo, é classificado como um exame voltado a condições clinicamente acionáveis.
O exame é indicado para adultos assintomáticos, a partir dos 18 anos, e analisa simultaneamente 117 genes por meio da técnica de Sequenciamento de Nova Geração (NGS). Esses genes estão organizados em três categorias principais:
- cânceres hereditários (42 genes): incluem BRCA1, BRCA2, TP53, MLH1, MSH2, entre outros;
- doenças cardiovasculares (53 genes): abrangem genes associados a cardiomiopatias, arritmias e dislipidemias familiares;
- outras condições genéticas (22 genes): incluem distúrbios metabólicos, neurológicos e hematológicos de origem monogênica.
O exame pode ser adquirido sem solicitação médica formal, mas recomenda-se fortemente o acompanhamento profissional, principalmente para interpretação dos achados genéticos e definição da conduta clínica a partir dos resultados.
Diferenciais técnicos e clínicos do exame GenomaCare
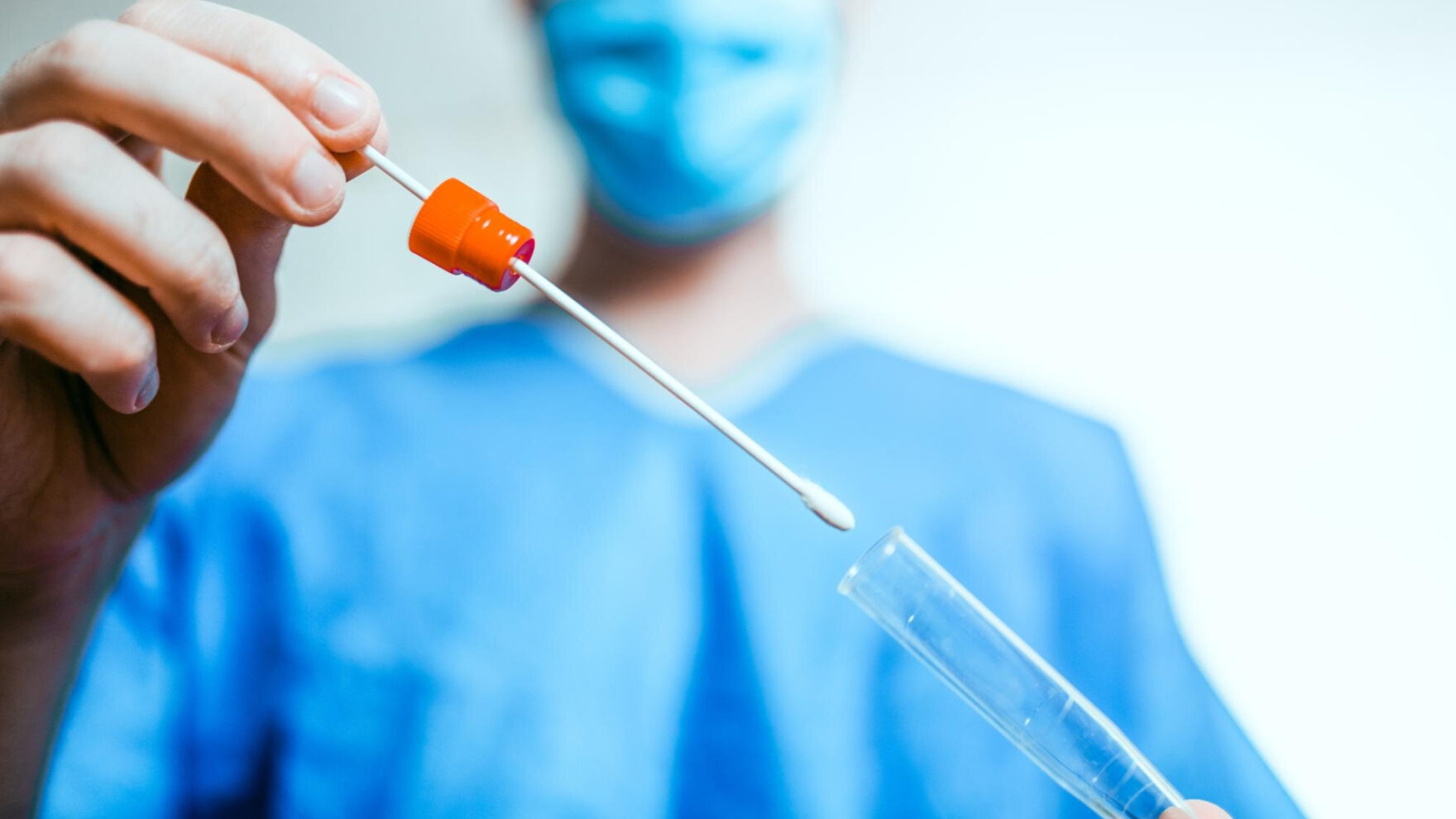
Um dos principais diferenciais do GenomaCare está na facilidade de coleta, feita por meio da coleta de saliva com swab bucal, garantindo método não invasivo, com alta aceitação e possibilidade de realização domiciliar.
Destacamos que o Sabin é reconhecido pela qualidade interpretativa dos laudos, elaborados com base nas recomendações mais recentes e validados por equipe especializada. Dessa forma, o laudo fornece não apenas a identificação das variantes genéticas relevantes, como também a correlação clínica com recomendações práticas, facilitando a tomada de decisão pelo médico assistente.
Esse tipo de suporte contribui para que o exame seja realmente aplicável, evitando dúvidas na interpretação e otimizando o tempo do profissional de saúde.
Aplicações clínicas do GenomaCare na medicina personalizada
A principal aplicabilidade do GenomaCare está na capacidade de personalizar condutas clínicas, com base em informações de risco individual. Nos casos de câncer hereditário, por exemplo, o exame pode identificar variantes em genes como BRCA1, BRCA2 e PALB2, que aumentam significativamente o risco de neoplasias de mama. A partir dessa informação, o médico pode antecipar a idade de início do rastreamento, indicar exames de imagem mais frequentes ou, em casos específicos, encaminhar para aconselhamento genético e discutir condutas redutoras de risco.
Em cardiologia, a identificação de variantes em genes como MYH7, KCNQ1 ou LMNA pode indicar risco para arritmias letais e miocardiopatias. Diante desse achado, o médico pode indicar exames de imagem cardíaca, teste de esforço, monitoramento ambulatorial ou mesmo implante de dispositivos, quando indicado, prevenindo eventos como a morte súbita.
Contraindicações do GenomaCare
Apesar da ampla aplicabilidade, o GenomaCare não é indicado para todos os casos. Ele não deve ser utilizado como exame diagnóstico em pacientes com suspeita clínica já estabelecida de condição genética. Nesses contextos, testes direcionados, solicitados pelo médico assistente, são os mais adequados.
Outras contraindicações incluem:
- pacientes receptoras de transplante de medula óssea (uma vez que o material genético analisado seria do doador);
- menores de 18 anos;
- indivíduos com histórico familiar fortemente sugestivo para síndrome genética, que se beneficiaram de testes diagnósticos (e não de triagem).
Nesses casos, é indicado o acompanhamento com geneticista clínico, que poderá orientar o exame mais apropriado conforme a suspeita diagnóstica.
Impacto do GenomaCare na jornada do paciente
O uso de exames genéticos em caráter preventivo pode contribuir para reduzir a morbimortalidade por doenças evitáveis, ao mesmo tempo em que otimiza recursos de saúde. Ao permitir a antecipação de condutas, o GenomaCare ajuda a evitar tratamentos de alto custo em fases tardias da doença e melhorar os prognósticos clínicos.
Além disso, o uso de exames de triagem genômica pode ser uma estratégia de apoio a políticas públicas de prevenção, notadamente em programas de rastreamento de câncer e cardiopatias em populações de risco.
A atuação do Sabin em genômica e na inovação diagnóstica
O Sabin tem se posicionado como referência em genômica clínica no Brasil, com investimento contínuo em infraestrutura laboratorial, tecnologia de sequenciamento e formação de equipes multiprofissionais especializadas em bioinformática, genética e interpretação clínica.
O laboratório oferece suporte técnico ao médico solicitante, desde a seleção adequada do exame até a interpretação dos achados, promovendo maior segurança nas decisões clínicas.
Adicionalmente, o Sabin disponibiliza materiais educacionais e apoia a formação médica continuada, com conteúdos científicos atualizados sobre genética clínica, reforçando seu compromisso com a educação médica e o cuidado integral ao paciente.
Acompanhe nosso canal do médico e atualize-se sobre temáticas que podem auxiliar a prática clínica. Conheça o portal dos Médicos | Sabin Diagnóstico e Saúde.
Referências:
Mighton, C., Shickh, S., Aguda, V., Krishnapillai, S., Adi-Wauran, E., & Bombard, Y. (2022). From the patient to the population: Use of genomics for population screening. Frontiers in genetics, 13, 893832. https://doi.org/10.3389/fgene.2022.893832
Samadder, N. J., Gay, E., Lindpere, V., Bublitz, M. L., Bandel, et al., (2024). Exome Sequencing Identifies Carriers of the Autosomal Dominant Cancer Predisposition Disorders Beyond Current Practice Guideline Recommendations. JCO precision oncology, 8, e2400106. https://doi.org/10.1200/PO.24.00106